Cosecha y clarificación a escala de laboratorio de vectores lentivirales mediante sistemas de filtración Sartoclear Dynamics Lab

Introducción
Con el advenimiento de la terapia génica y de células modificadas genéticamente los virus se han convertido en herramientas fundamentales en la medicina. La terapia génica tiene un importante potencial terapéutico para el tratamiento de muchas enfermedades hereditarias y adquiridas¹, con tres mil ensayos clínicos registrados en curso que utilizan vectores virales, entre los cuales alrededor del 10% se realizan con vectores lentivirales². Actualmente, hay más de dos mil productos únicos de células modificadas genéticamente en desarrollo y ya se han aprobado cuatro terapias CAR-T para tratar indicaciones oncológicas. La perspectiva prometedora de los ensayos clínicos en curso sobre terapia génica y de células modificadas³,⁴ significa que existe una fuerte demanda de métodos escalables y rentables para la producción y purificación de vectores virales⁵.
Los vectores lentivirales (LV) suelen producirse mediante la transfección transitoria de células HEK293T con múltiples plásmidos vectores⁶,⁷. El virus se libera en el sobrenadante, por lo tanto las células se deben eliminar del caldo de cultivo. Uno de los desafíos en la investigación CAR-T es la falta de un método establecido de clarificación de LV considerado estándar de oro. El objetivo del proceso de clarificación es eliminar los principales contaminantes y reducir la turbidez de la solución manteniendo al mismo tiempo la actividad viral. A escala de laboratorio, la clarificación se suele realizar mediante centrifugación del caldo de fermentación, complementada con una microfiltración posterior del sobrenadante¹,⁸,⁹. Simplificar la cosecha y la clarificación utilizando solo una filtración por membrana de un solo paso, lo que se puede lograr mediante el uso de auxiliares de filtración, mejoraría la eficiencia de la purificación de LV y la transducción de células T.
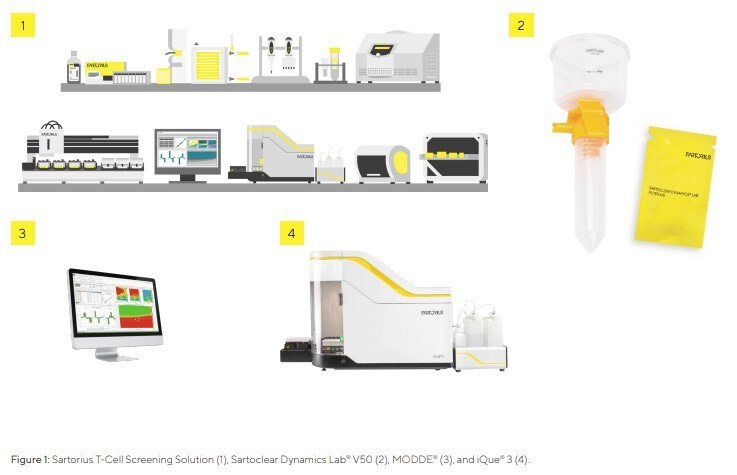
Para simplificar los flujos de trabajo de investigación CAR-T, la solución Sartorius T-Cell Screening ofrece una forma semiautomatizada y multiplexada de descubrir nuevos objetivos y desarrollar construcciones CAR eficientes (Figura 1). En particular, la serie Sartoclear Dynamics Lab de productos de filtración utilizados para la clarificación del caldo de cultivo celular se desarrolló para facilitar un flujo de trabajo de cosecha de vectores virales rápido y eficiente y se basa en el principio de la filtración dinámica con carga de tierra de diatomeas. El auxiliar de filtración de tierra de diatomeas (DE) consiste en restos esqueletales fusionados de diatomeas con una estructura altamente porosa¹⁰. Después del proceso upstream, el caldo de cultivo se mezcla primero con un auxiliar de filtración y luego se aplica a una membrana filtrante. La DE forma una capa porosa prácticamente incompresible, y su alta porosidad permite que el líquido fluya alrededor de las partículas, evitando la obstrucción del filtro¹¹. El uso de auxiliares de filtración elimina el paso de centrifugación y reduce el tiempo de procesamiento.
Materiales y métodos
El vector lentiviral se expresó mediante transfección transitoria de células HEK293T/17 SF cultivadas en suspensión en el biorreactor desechable UniVessel de 2 L (Sartorius), con cuatro plásmidos que codifican los genes lentivirales esenciales, tal como se describe en detalle en Labisch et al.¹²
La clarificación de muestras de 50 mL de caldo de cultivo de LV se realizó utilizando la versión Sartoclear Dynamics Lab V50 de 0,45 μm de polisulfona de éter (PES) (Sartorius).
El kit Sartoclear Dynamics Lab V50 contiene unidades de filtración al vacío Sartolab RF50, que constan de un embudo, un tubo cónico de 50 mL y un conector para la conexión al vacío. El kit se suministra con cantidades estándar de 1 g de DE (Sartorius, SDLV-0050-01F0-2) o 2 g de DE (Sartorius, SDLV-0050-02F0-2) para la filtración de hasta 50 mL. Se probaron concentraciones de DE entre 5 g/L y 40 g/L de caldo de cultivo. Se añadió DE a 50 mL de caldo de cultivo y se mezcló para obtener una suspensión homogénea, que luego se filtró inmediatamente. Además, se realizó la clarificación de 50 mL de caldo de cultivo sin DE mediante un método de dos pasos: centrifugación durante 5 min a 800 × g y posterior filtración a través de un Sartolab RF50 con una membrana PES de 0,45 μm (Sartorius, 180F01---------2).
Para determinar la capacidad del filtro, la clarificación se efectuó hasta que se produjo la obstrucción del filtro determinándose el volumen del filtrado. La filtración al vacío se realizó con el Sartolab MultiStation (Sartorius, SDLC01), un soporte diseñado específicamente para alojar entre una y seis unidades Sartolab RF50 lo que permite la filtración simultánea de hasta seis muestras.
Se utilizó un enfoque de diseño de experimentos (DOE) para optimizar las condiciones de clarificación. La concentración de DE se varió entre 5 g/L, 12,5 g/L y 20 g/L, y el tiempo de contacto entre 0, 10 y 20 minutos. Los experimentos se planificaron como un diseño factorial completo con cuatro puntos centrales y se evaluaron utilizando el software MODDE™ (Sartorius). Los parámetros analíticos empleados para determinar el rendimiento de la clarificación fueron los siguientes: medición de la turbidez utilizando un turbidímetro Orion™ AQUAfast AQ3010 (Thermo Fisher Scientific), concentración total de ADN bicatenario (ensayo Quant-iT™ PicoGreen™, Thermo Fisher Scientific) y concentración total de proteínas (kit de ensayo proteico Pierce™ Coomassie Bradford, Thermo Fisher Scientific), antes (material centrifugado) y después de la filtración. Además, el título de partículas de LV se determinó mediante ELISA p24 (QuickTiter™ Lentivirus Titer Kit, Cell Biolabs). El título de partículas lentivirales infecciosas se midió mediante la transducción de células HEK293T adherentes con muestras virales y la medición de la expresión del transgén (constructo CAR-CD19) por citometría de flujo con el iQue Screener PLUS (Sartorius), tal como se describió anteriormente¹².
Resultados y discusión
Evaluación del impacto de la concentración de DE y el tiempo de contacto con DE sobre la turbidez, el título infeccioso y el tiempo de filtración en un estudio DOE utilizando MODDE
Para investigar el efecto de la DE en la clarificación de LV, se seleccionaron la concentración de DE y el tiempo de contacto con DE como factores en un enfoque DOE para evaluar su influencia sobre la turbidez, el título infeccioso y el tiempo de filtración. La densidad celular total del caldo de cultivo utilizado en las corridas de filtración del DOE fue de 3,7 × 10⁶ células/mL, con una turbidez de 382 NTU.
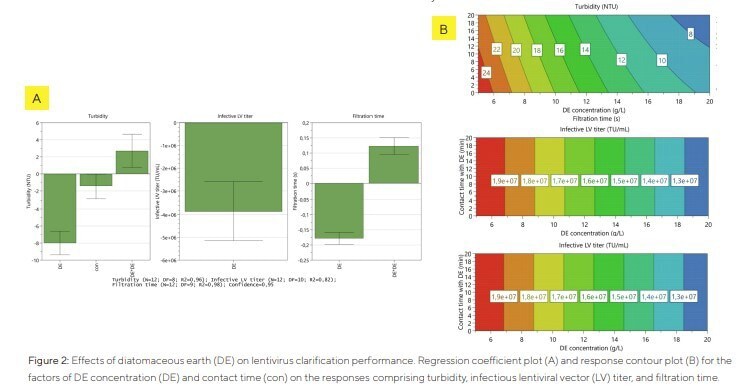
La Figura 2 muestra que las respuestas relativas al título infeccioso y al tiempo de filtración solo se ven afectadas por el factor concentración de DE. A medida que aumenta la concentración de DE el título infeccioso disminuye linealmente. En cuanto al tiempo de filtración, existe un término cuadrático para la concentración de DE, lo que da lugar a una reducción del tiempo de filtración a medida que aumenta la concentración de DE dentro del rango de prueba definido. La turbidez se redujo linealmente al prolongarse el tiempo de contacto de la muestra con la DE. Además, al aumentar la concentración de DE, la turbidez disminuyó, siendo este último el factor con mayor efecto.
Evaluación del impacto del Sartoclear Dynamics Lab V50 en el tiempo de procesamiento
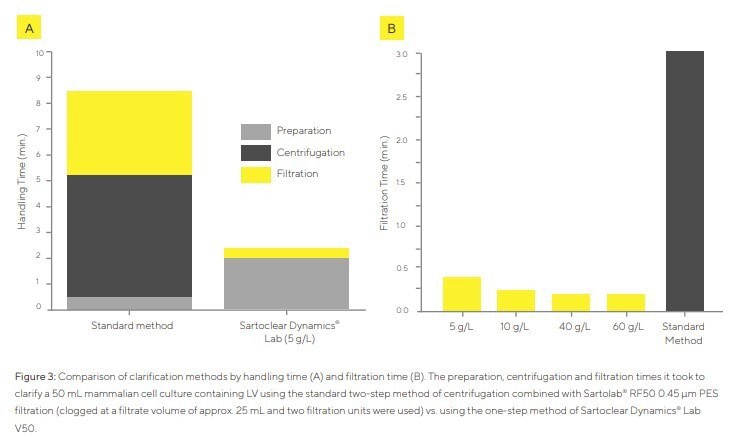
La manipulación del kit Sartoclear Dynamics Lab V50 con diferentes concentraciones de DE se comparó con la microfiltración del sobrenadante centrifugado mediante Sartolab RF50 (método estándar de dos pasos). Tras la cosecha del cultivo celular, la densidad celular para los experimentos de manipulación fue de 1,11 × 10⁶ células/mL y la turbidez de 141 NTU. El tiempo total de procesamiento se dividió en tiempo de preparación (medición de volúmenes, retirada del sobrenadante tras la centrifugación, pesado y adición de DE), tiempo de centrifugación y tiempo de filtración.
Durante la clarificación del sobrenadante centrifugado, el primer filtro Sartolab RF50 se obstruyó tras aproximadamente 25 mL. Por tanto, fue necesario un segundo filtro, lo que implicó transferir la solución restante, dificultando considerablemente el manejo. El uso de Sartoclear Dynamics Lab V50 redujo el tiempo de preparación al eliminar la necesidad de un paso de centrifugación (Figura 3A). El tiempo total de manipulación se redujo 3,8 veces en comparación con el método estándar. El tiempo de filtración dependió de la concentración de DE: fue de 25 s para 5 g/L y se redujo a 13 s para 60 g/L (Figura 3B).
Evaluación del impacto del Sartoclear Dynamics Lab V50 en la turbidez y la capacidad del filtro
La clarificación se realizó bien con Sartoclear Dynamics Lab V50 y 5 g/L de DE, o bien con el método convencional de dos pasos con centrifugación y filtración. El caldo de cultivo que contenía lentivirus usado para la determinación de capacidad del filtro tenía una densidad celular total de 3,7 × 10⁶ células/mL y una turbidez de 398 NTU en el momento de la cosecha.
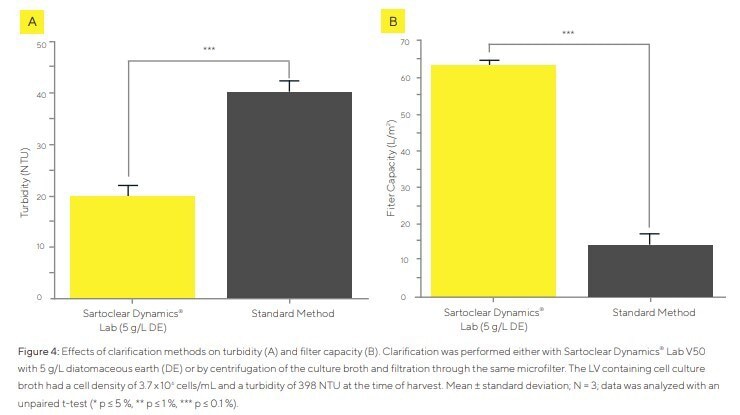
Según la Figura 4A, el método estándar de centrifugación seguida de filtración da como resultado una turbidez significativamente mayor de 43 NTU (reducción del 89%), mientras que Sartoclear Dynamics Lab V50 redujo la turbidez en un 95%, hasta 21 NTU. Las capacidades de filtración se determinaron utilizando solo la concentración mínima de DE (5 g/L). La filtración se continuó hasta que se produjo la obstrucción del filtro. El método convencional, con centrifugación para eliminar células y posterior filtración, produjo un rápido taponamiento tras solo 33 mL. El uso de 5 g/L de DE aumentó enormemente el volumen máximo filtrable, superando más de dos veces la capacidad del dispositivo de 50 mL. Las capacidades de filtración aumentaron significativamente con 5 g/L de DE (Figura 4B). En contraste, las capacidades de filtración fueron bajas con el método convencional (15 L/m²). Con 5 g/L de DE, las capacidades aumentaron hasta unos 63 L/m². Tras la clarificación con DE, el título infeccioso de LV fue normalmente del 75% o superior en comparación con el material centrifugado.
Evaluación del impacto de Sartoclear Dynamics Lab V50 en la eliminación de impurezas
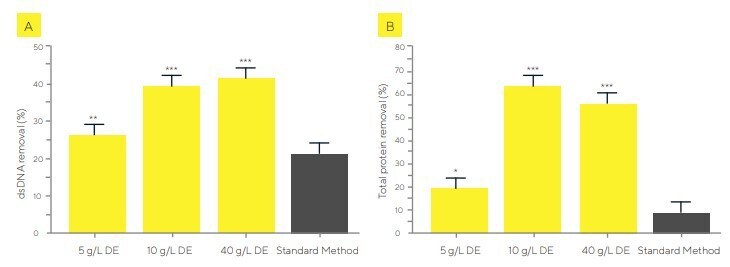
En un experimento independiente, se analizó el potencial de Sartoclear Dynamics Lab V50 para eliminar impurezas relacionadas con el proceso mediante la cuantificación de la eliminación total de proteínas y de ADN bicatenario (dsDNA) (Figura 5).
Una concentración de DE de hasta 10 g/L aumentó la eliminación de proteínas y dsDNA, pero concentraciones más altas, entre 10 g/L y 40 g/L, no produjeron mejoras adicionales en la eliminación de impurezas. En contraste, el uso de Sartoclear Dynamics Lab V50 dio lugar a una eliminación significativamente mayor de impurezas en comparación con el método estándar de dos pasos mediante centrifugación y filtración.
Conclusión
Los sistemas de filtración Sartoclear Dynamics Lab permiten la clarificación de cultivos celulares de mamíferos que contienen LV sin necesidad de centrifugación. En comparación con el método estándar, Sartoclear Dynamics Lab V50 proporcionó una mejor reducción de turbidez, una mayor eliminación de contaminantes y una mayor capacidad de membrana. Esto subraya la idoneidad de los sistemas de filtración Sartoclear Dynamics™ Lab para la cosecha y clarificación de vectores lentivirales. Sin embargo, es necesario ajustar la concentración de DE para recuperar altos rendimientos de LV y evitar pérdidas debidas al uso de cantidades inapropiadamente altas de DE. El kit Sartoclear Dynamics Lab V50 con DE permite al técnico de laboratorio realizar una filtración clarificante en un solo paso que no solo facilita una manipulación más rápida y segura, sino que también reduce la cantidad de materiales de laboratorio utilizados. El kit permite seleccionar una cantidad optimizada de DE que aumenta notablemente la capacidad del filtro, garantizando así un proceso de clarificación de lentivirus eficiente y robusto en terapias génicas y de células modificadas.
Referencias
1 Segura, M. M., Kamen, A. A., and Garnier, A. 2011. Overview of current scalable methods for purification of viral vectors. Methods in molecular biology (Clifton, N.J.) 737, 89–116.
2 John Wiley & Sons, Inc. 2019. Gene therapy trials worldwide. John Wiley & Sons, Inc, Hoboken, NJ, USA. Journal of Gene Medicine. h t t p://w w w.abedia.com/ wiley/vectors.php. Accessed 5 May 2020.
3 Hanna, E., Rémuzat, C., Auquier, P., and Toumi, M. 2017. Gene therapies development: slow progress and promising prospect. Journal of market access & health policy 5, 1, 1265293.
4 Herzog, R. W., Cao, O., and Srivastava, A. 2010. Two decades of clinical gene therapy--success is finally mounting. Discovery medicine 9, 45, 105–111.
5 Ruscic, J., Perry, C., Mukhopadhyay, T., Takeuchi, Y., and Bracewell, D. G. 2019. Lentiviral Vector Purification Using Nanofiber Ion-Exchange Chromatography. Molecular therapy. Methods & clinical development 15, 52–62.
6 Merten, O.-W., Schweizer, M., Chahal, P., and Kamen, A. 2014. Manufacturing of viral vectors: part II. Downstream processing and safety aspects. Pharmaceutical Bioprocessing 2, 3, 237–251.
7 Sakuma, T., Barry, M. A., and Ikeda, Y. 2012. Lentiviral vectors: basic to translational. The Biochemical journal 443, 3, 603–618.
8 Bauler, M., Roberts, J. K., Wu, C.-C., Fan, B., Ferrara, F., Yip, B. H., Diao, S., Kim, Y.-I., Moore, J., Zhou, S., Wielgosz, M. M., Ryu, B., and Throm, R. E. 2020. Production of Lentiviral Vectors Using Suspension Cells Grown in Serum-free Media. Molecular therapy. Methods & clinical development 17, 58–68.
9 Rodrigues, T., Carrondo, M. J. T., Alves, P. M., and Cruz, P. E. 2007. Purification of retroviral vectors for clinical application: biological implications and technological challenges. Journal of biotechnology 127, 3, 520–541.
10 Bakr, H. E. G. M. 2010. Diatomite: Its Characterization, Modifications and Applications. Asian J. of Materials Science 2, 3, 121–136.
11 Grauf, M., Lagrange, B., and Schöne, K. 2018. Simplified Small-Scale Harvest of CHO Cells for mAb Analytics. Genetic Engineering & Biotechnology News 38, 5, 22– 23.
12 Labisch, J. J., Bollmann, F., Wolff, M. W., and Pflanz, K. 2021. A new simplified clarification approach for lentiviral vectors using diatomaceous earth improves throughput and safe handling. Journal of biotechnology, 326, 11–20.
Abreviaturas
CAR - Receptor de antígeno quimérico
(ds)DNA - ADN (bicatenario) desoxirribonucleico
DE - Tierra de diatomeas
DOE - Diseño de experimentos
HEK - Células de riñón embrionario humano
LV - Vector lentiviral
PES - Polietersulfona
TU - Unidades de transducción
VP - Partículas virales