
Introducción
Los virus nuevos, denominados virus emergentes, representan una amenaza para la salud humana de una magnitud que no debe subestimarse. Estos virus han adquirido la capacidad de infectar a los seres humanos ya sea como consecuencia de la transmisión entre especies o de cambios naturales en el genoma viral¹. Las infecciones causadas por virus emergentes a menudo provocan enfermedades graves o incluso la muerte, ya que el sistema inmunitario humano puede no ser capaz de combatir un virus desconocido, especialmente si es de origen zoonótico (véase la bibliografía para más información²).
Diversos factores favorecen la aparición y propagación de los virus emergentes³. Entre ellos se incluyen factores ecológicos, como la deforestación para obtener nuevas tierras destinadas al desarrollo, así como nuestro estilo de vida caracterizado por la movilidad global y el comercio internacional. De este modo, la pérdida de hábitat incrementa la probabilidad de que las personas, las mascotas y los animales de granja entren en contacto con especies silvestres que originalmente habitaban zonas aisladas y que, por lo tanto, no habían sido encontradas previamente como hospedadores naturales de virus emergentes. Además, las circunstancias propias de una sociedad globalizada, que implican un aumento de los viajes, también permiten la diseminación de virus patógenos en todo el mundo, incluso antes de la aparición de síntomas clínicos.
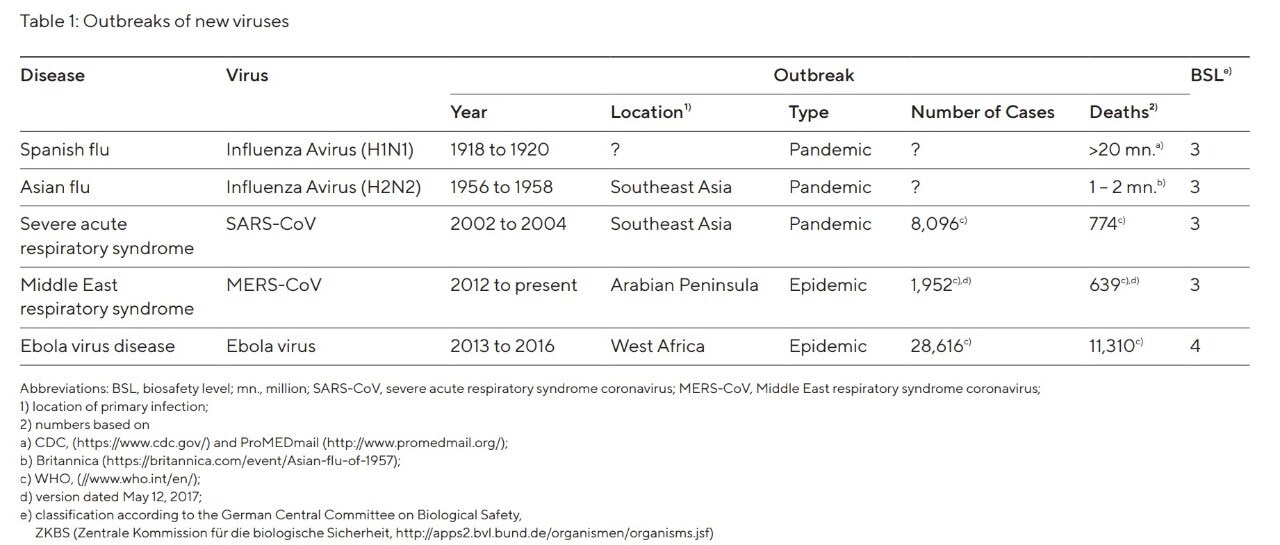
Durante los últimos 100 años se han producido múltiples introducciones de virus emergentes en la población humana, lo que ha dado lugar a epidemias locales o brotes a escala mundial (pandemias; véase la Tabla 1). En particular, el virus del Ébola ha suscitado recientemente preocupación en todo el mundo, ya que la epidemia de Ébola en África Occidental, que se cobró más de 11.000 vidas, demostró de manera devastadora el peligro que representan los virus emergentes⁴. La investigación que involucra virus emergentes suele limitarse a laboratorios de alta contención con niveles de bioseguridad (BSL) 3 y 4 (véase la Tabla 1). El trabajo en laboratorios BSL-4 es extremadamente laborioso, costoso y solo está permitido en unos pocos lugares, lo que dificulta lograr avances científicos rápidos en la caracterización de patógenos virales y el desarrollo de fármacos antivirales.
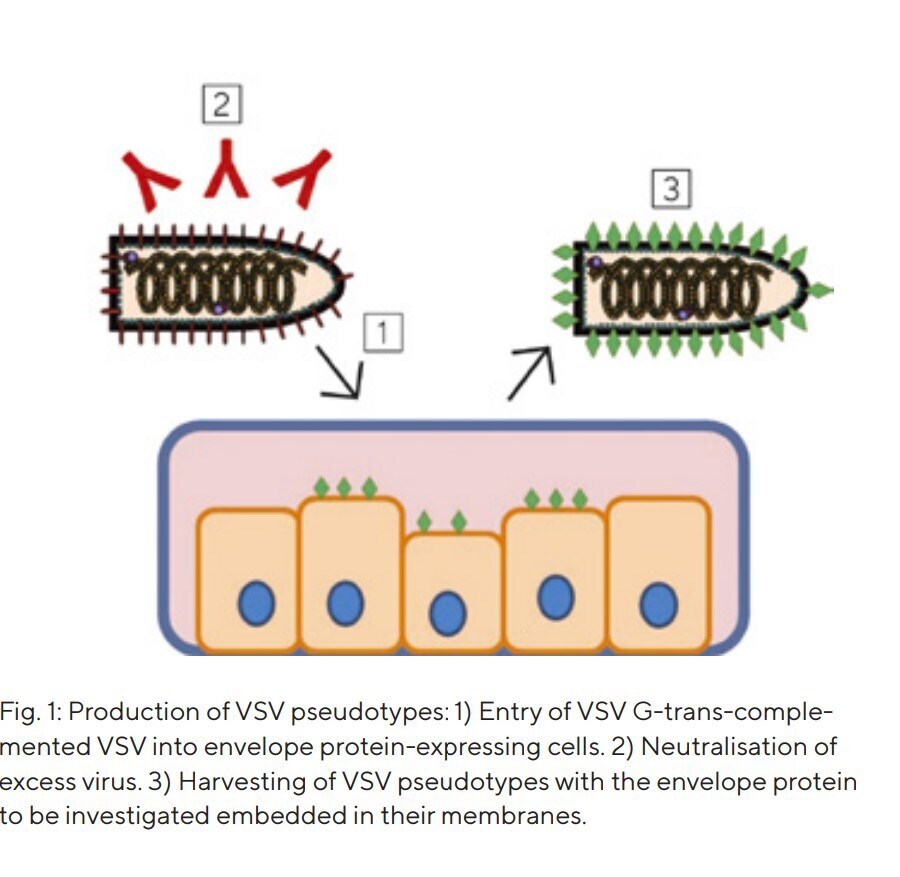
Dada esta situación, los pseudotipos virales ofrecen una opción atractiva para estudiar de manera segura y eficiente la entrada de virus altamente patógenos en las células. Esto es posible porque no se analiza el patógeno completo, sino únicamente los componentes que median la entrada en la célula huésped, es decir, las proteínas de la envoltura. Estas representan la clave para la entrada del virus en las células. En el caso de los pseudotipos virales, las proteínas de la envoltura de virus altamente patógenos se incorporan a un virus portador (pseudotipado), que no puede replicarse de forma autónoma, es decir, es deficiente en replicación. Los sistemas comúnmente utilizados para el pseudotipado se basan en rabdovirus (por ejemplo, el virus de la estomatitis vesicular, VSV; Fig. 1) y retrovirus.
El objetivo de este estudio fue verificar si la entrada mediada por proteínas de la envoltura de los pseudotipos virales refleja la entrada en la célula huésped de los virus intactos. Además, esta investigación se diseñó para determinar la influencia que tiene el nivel de pureza de los reactivos utilizados, en este caso el agua de laboratorio, sobre la producción de pseudotipos virales.
Materiales y Métodos
Cultivo celular, plásmidos de expresión y transfección: Las células HEK-293T, MDCKII y Vero E6 se incubaron en medio Eagle modificado de Dulbecco (DMEM) suplementado con 10% de suero fetal bovino (FCS) y 1% de solución de penicilina/estreptomicina a 37 °C y 5% de CO₂. Para el pasaje y la siembra, las células se lavaron con solución salina tamponada con fosfato (PBS) y se desprendieron mediante incubación con tripsina | EDTA.
Para producir pseudotipos de VSV, se utilizaron plásmidos de las siguientes proteínas de envoltura viral como vectores de expresión: glicoproteína del VSV (VSV G), glicoproteína del virus del Ébola (EBOV GP), glicoproteína espiga del coronavirus del síndrome respiratorio de Oriente Medio (MERS-CoV S), hemaglutinina (HA) y neuraminidasa (NA) del virus de la influenza A responsable de la pandemia de la “gripe española”, H1N1 (1918). Además, se empleó un plásmido de expresión para la dipeptidil peptidasa 4 (DPP4). Se utilizó un plásmido de expresión vacío como control. Las células HEK-293T se transfectaron mediante precipitación con calcio | fosfato, utilizando tampones y soluciones preparados con agua desmineralizada o con agua ultrapura Sartorius Arium Pro VF.
Producción de agua ultrapura
El agua ultrapura Arium Pro VF utilizada se produjo según lo descrito por Nitzki y Herbig (2013)⁵. Esta agua presenta un contenido de TOC (carbono orgánico total, es decir, carbono unido orgánicamente) de hasta < 2 ppb y una conductividad de 0,055 μS/cm (correspondiente a una resistividad de 18,2 MΩ × cm), compensada a 25 °C.
Producción de pseudotipos de VSV
Para la generación de pseudotipos de VSV se empleó un vector de VSV deficiente en replicación, en el cual la información genómica de la glicoproteína del VSV, VSV G, fue sustituida por dos genes reporteros, es decir, marcos de lectura abiertos (ORF) que codifican la proteína verde fluorescente (GFP) y la luciferasa de luciérnaga (fLUC). Para propagar este virus (VSV*ΔG-fLUC), la VSV G debe suministrarse en trans (por ejemplo, mediante la transfección de un plásmido de expresión). Los pseudotipos de VSV se produjeron como se describió en Hoffmann et al. (2016)⁶.
Pretratamiento de las células diana con sialidasa o inhibidores:
Las células MDCKII se trataron con 200 mU de sialidasa recombinante para eliminar los ácidos siálicos terminales de las glicoproteínas y glicolípidos de la membrana plasmática. Para evaluar si la entrada mediada por proteínas de la envoltura de los pseudotipos de VSV en las células depende de un pH ácido y de la actividad de proteasas cisteínicas celulares, las células Vero E6 se incubaron con 50 nM de bafilomicina A1 o 50 μM de E-64d. Los compuestos químicos empleados se diluyeron en medio de cultivo celular; la incubación se llevó a cabo durante 2 horas a 37 °C y 5% de CO₂. Las células no tratadas sirvieron como controles.
Análisis de la entrada en la célula huésped mediada por proteínas de la envoltura:
Las células diana se incubaron con pseudotipos de VSV durante 1 hora, tras lo cual se lavaron con PBS y se incubaron adicionalmente con medio de cultivo celular durante 16–20 horas. Posteriormente, las células se lisaron utilizando un tampón de lisis de luciferasa y la actividad de la luciferasa en los lisados celulares se midió en un quimioluminómetro utilizando kits de ensayo disponibles comercialmente para evaluar la eficiencia de la transducción (es decir, la entrada de los pseudotipos en la célula huésped) mediada por las proteínas de la envoltura.
Resultados
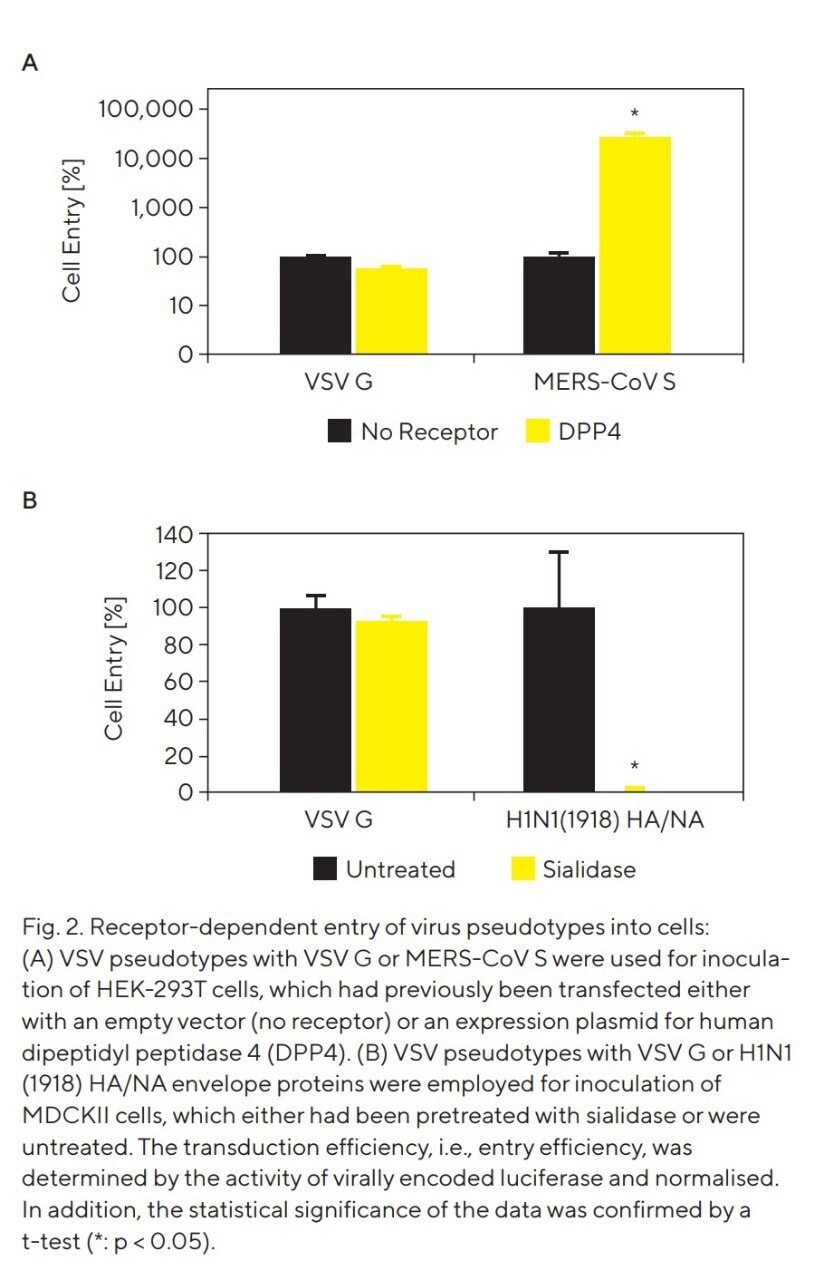
Se sabe que el coronavirus del síndrome respiratorio de Oriente Medio (MERS-CoV, anteriormente denominado coronavirus humano, EMC = hCoV-EMC) se une a la superficie celular mediante la interacción entre la glicoproteína espiga viral (S) y la proteína de membrana celular dipeptidil peptidasa 4 (DPP4), lo que permite la entrada en la célula⁷. Para confirmar si esto también se aplica en el contexto de los pseudotipos de VSV, las células diana se transfectaron con un vector de expresión para DPP4 o con un plásmido de expresión vacío (sin receptor). Como se esperaba, la expresión dirigida de DPP4 condujo a un aumento significativo de la entrada en la célula huésped de los pseudotipos de VSV cuando estos contenían la proteína S de MERS-CoV integrada en su envoltura (véase Fig. 2A).
Los virus de la influenza A, agentes causantes de la enfermedad gripal, requieren estructuras terminales de azúcares, los llamados ácidos siálicos, que aparecen como modificaciones naturales en las glicoproteínas y glicolípidos de la membrana celular, como receptores para mediar la entrada en las células diana (véase la bibliografía para más información⁸). Para estudiar si la incorporación de proteínas de la envoltura del virus de la influenza A en pseudotipos de VSV también da lugar a una entrada celular dependiente del ácido siálico, se emplearon pseudotipos de VSV con HA/NA de H1N1 (1918), y los ácidos siálicos se eliminaron enzimáticamente de la superficie de las células diana. Como se esperaba, la eliminación de los ácidos siálicos provocó una disminución drástica de la entrada en la célula huésped de los pseudotipos de VSV que contenían HA/NA de H1N1 (1918) en su envoltura (véase Fig. 2B). Este hallazgo confirma que los pseudotipos virales reflejan el mecanismo de entrada en las células de los virus auténticos de la influenza A.
La activación de la glicoproteína del virus del Ébola durante la entrada celular es dependiente del pH y requiere la actividad de proteasas cisteínicas
La glicoproteína del virus del Ébola (EBOV GP) se modifica postraduccionalmente para contener múltiples oligosacáridos, y se cree que esta densa acumulación de glicanos protege al virus de una detección eficaz por parte del sistema inmunitario humano⁹. Sin embargo, durante la entrada en la célula huésped, debe eliminarse una parte de la EBOV GP que contiene la mayoría de las modificaciones de azúcares¹⁰. Este cebado funcional está mediado por proteasas cisteínicas celulares¹¹ que se encuentran en las vesículas endosómicas y que solo están activas a un pH endosomal bajo.
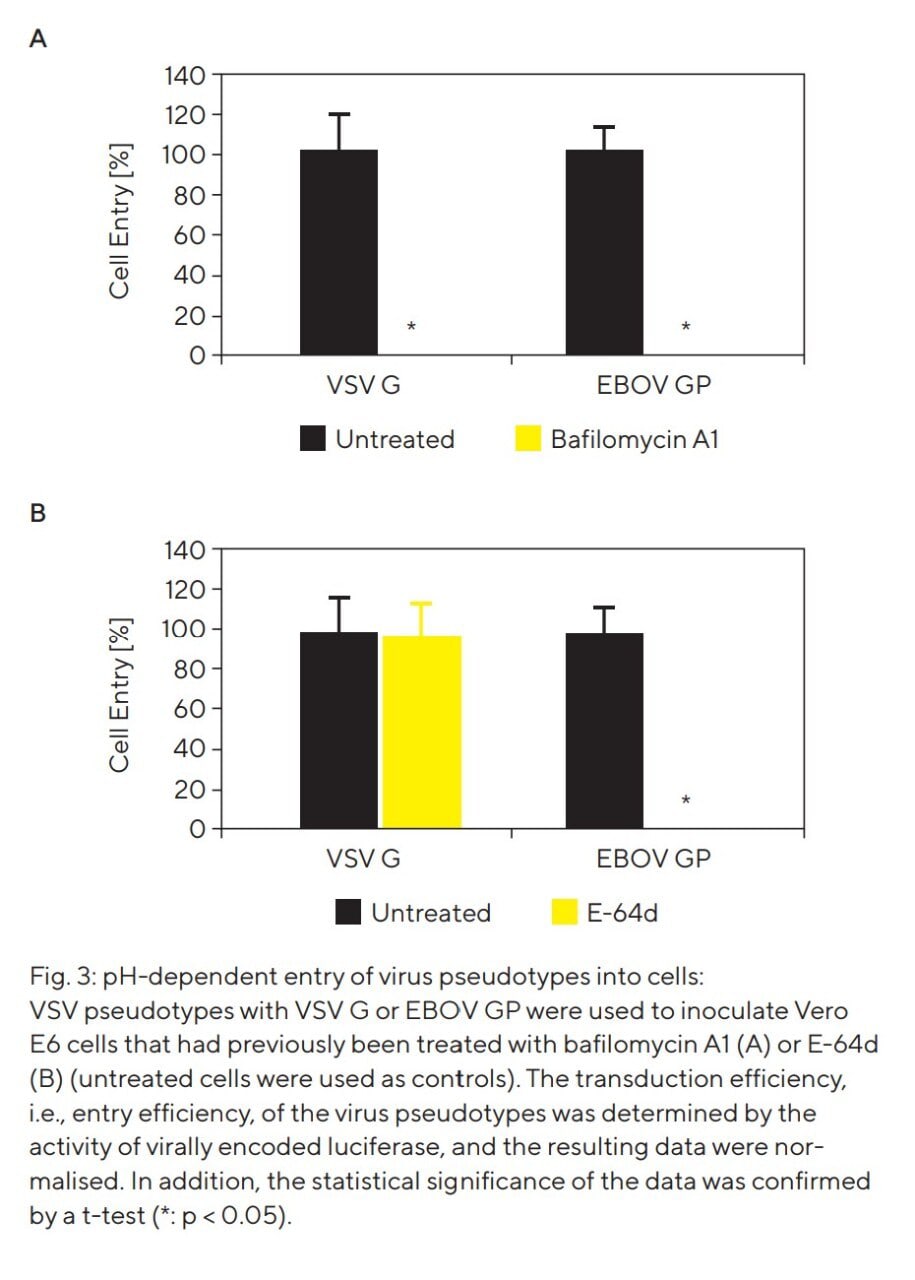
A continuación, investigamos si la entrada mediada por la EBOV GP de pseudotipos de VSV también depende de la actividad de las proteasas cisteínicas celulares y de un pH bajo. Con este fin, se produjeron pseudotipos de VSV con EBOV GP incorporada en su envoltura y posteriormente se utilizaron para inocular células diana que habían sido incubadas previamente con bafilomicina A1 (que impide la acidificación dentro de los endosomas mediante el bloqueo de bombas de protones) o con un inhibidor de proteasas cisteínicas (E-64d). Los resultados mostraron que la entrada celular mediada por la EBOV GP en el contexto de los pseudotipos de VSV también depende de un entorno ácido (véase Fig. 3A) y de la actividad de las proteasas cisteínicas (véase Fig. 3B). Además, se pudo demostrar que el tratamiento con E-64d bloquea específicamente la entrada celular impulsada por la EBOV GP, ya que la entrada mediada por pseudotipos con VSV-G es independiente de las proteasas cisteínicas, aunque depende de un pH endosomal bajo.
El nivel de pureza del agua de laboratorio utilizada influye en la calidad de los pseudotipos de VSV
Después de que en los ensayos previos se demostrara que los pseudotipos de VSV son modelos adecuados para estudiar la entrada en la célula huésped de virus altamente patógenos, la siguiente cuestión a esclarecer fue la influencia específica que ejerce el nivel de pureza del agua de laboratorio utilizada sobre la calidad de los pseudotipos de VSV. Durante la producción de pseudotipos de VSV se emplean diversos tampones y soluciones, todos ellos preparados con agua. Sin embargo, debe tenerse en cuenta que no cualquier tipo de agua es suficiente para la preparación de estos reactivos. Por el contrario, es necesario seleccionar el nivel de pureza adecuado para su uso en el laboratorio.
Para investigar si el uso de agua ultrapura da lugar a pseudotipos de VSV de mayor calidad, se generaron dos lotes de pseudotipos de VSV en un experimento paralelo: un lote se preparó utilizando agua desmineralizada procedente de un sistema central de suministro de agua de laboratorio (conductividad de 3,7–4,1 μS/cm a 19°C) como disolvente básico para todas las soluciones y tampones, mientras que otro lote se generó utilizando soluciones y tampones preparados con agua ultrapura Arium Pro VF (conductividad de 0,055 μS/cm compensada a 25°C). Se analizaron como proteínas de la envoltura la EBOV GP y la MERS-CoV S. Tras la producción paralela de los pseudotipos de VSV manteniendo condiciones de incubación idénticas, se inocularon las células diana y se cuantificó la entrada mediada por proteínas de la envoltura de los pseudotipos de VSV.
Este diseño experimental demostró que la entrada en la célula huésped (como parámetro del grado de calidad) de los pseudotipos de VSV producidos utilizando agua ultrapura Arium Pro VF como disolvente básico para todos los tampones y soluciones fue significativamente mayor en comparación con la de los pseudotipos para cuya producción se empleó agua desmineralizada (Fig. 4).
Discusión
Durante este estudio, se produjeron pseudotipos virales basados en un virus de la estomatitis vesicular (VSV) deficiente en replicación, y se investigaron las proteínas de la envoltura de diversos virus altamente patógenos. Demostramos que la entrada en la célula huésped dependía de las mismas moléculas receptoras y de los mismos procesos bioquímicos descritos para los virus auténticos. Además, demostramos que el uso de agua ultrapura para la producción de pseudotipos de VSV dio lugar a una optimización de este proceso. Investigaciones futuras deberían diseñarse para esclarecer en qué se basa esta observación: ¿se debe a una mayor cantidad de pseudotipos de VSV producidos, a una entrada celular más eficiente o a una mayor estabilidad de los pseudotipos? Por ejemplo, puede especularse que la ausencia de sales, proteinasas o lipasas cuando se utiliza agua ultrapura aumenta la estabilidad de los pseudotipos de VSV.
En conclusión, se puede afirmar que los pseudotipos virales son herramientas importantes para investigar la entrada en la célula huésped de virus altamente patógenos. Dado que estos pseudotipos virales no restringen la investigación sobre virus altamente patógenos a laboratorios BSL-3 o BSL-4, se permite que un mayor número de centros científicos lleven a cabo este tipo de investigaciones.
Como resultado, la entrada celular de los virus emergentes se puede caracterizar y se puede desarrollar con mayor rapidez procedimientos de detección adecuados y estrategias antivirales (medicamentos, vacunas). El uso de pseudotipos también reduce la considerable intensidad laboral requerida en los laboratorios de alta contención que exigen trajes de protección corporal completa, así como los elevados costes y las limitaciones inherentes a este tipo de trabajo (por ejemplo, la falta de acceso a equipos que no se encuentran directamente dentro del laboratorio de alta contención).
Además, en comparación con virus auténticos altamente patógenos, los pseudotipos virales minimizan el riesgo de infección del personal de laboratorio tras una exposición no intencionada, lo que representa un aspecto de seguridad significativo.
La optimización del proceso de producción, por ejemplo mediante el uso de reactivos de alta pureza, en particular los basados en agua, puede contribuir adicionalmente a mejorar la sensibilidad de los procedimientos de ensayo posteriores, aumentar las cantidades de producción y, de este modo, reducir aún más los costes de producción.
Referencias
1 Li, W. et al. Animal origins of the severe acute respiratory syndrome coronavirus: Insight from ACE2-Sprotein interactions. Journal of Virology 2016; 80: 4211–4219.
2 Mandl, J. et al. Reservoir host immune responses to emerging zoonotic viruses. Cell 2015; 160: 20–35.
3 Morse, S. S. Factors in the emergence of infectious diseases. Emerging Infectious Diseases 1995; 1: 7–15.
4 Shiwani, H. A. et al. An update on the 2014 Ebola outbreak in Western Africa. Asian Pacific Journal of Tropical Medicine 2017; 10: 6–10.
5 Nitzki, F., Herbig, E. In situ Hybridisierung – Die Bedeutung von Reinstwasser für RNA Technologien”, GIT Labor-Fachzeitschrift 57. Jahrgang, 3; 2013 [also available in English: In Situ Hybridization: The Importance of Ultrapure Water for RNA Technologies].
6 Hoffmann, M. et al. The glycoproteins of all filovirus species use the same host factors for entry into bat and human cells but entry efficiency is species dependent. PLoS One; 2016, Vol. 11.
7 Raj, V. S. et al. Dipeptidyl peptidase 4 is a functional receptor for the emerging human coronavirus-EMC. Nature 2013; 495: 251–254.
8 De Graaf, M., Fouchier, R. A. M. Role of receptor binding specificity in influenza A virus transmission and pathogenesis. The EMBO Journal 2014; 33: 781–935.
9 Cook, J. D., Lee, J. E. The secret life of viral entry glycoproteins: Moonlighting in immune evasion. PLoS Pathogens 2013; Vol. 9.
10 White, J. M., Schornberg, K. L. A new player in the puzzle of filovirus entry. Nature Reviews Microbiology 2012; 10: 317–322.
11 Chandran, K. et al. Endosomal proteolysis of the Ebola virus glycoprotein is necessary for infection. Science 2005; 308: 1643–1645.
